(关注原因:短期,FDA于11月底组织讨论默沙东/默克新冠药物EUA授权;按照时间线推算,预计圣诞节前后将讨论辉瑞EUA授权)
1、辉瑞新冠口服药Paxlovid,FDA授权预期
1)默沙东/默克于10月11日提交新冠药物莫纳皮拉韦(Molnupiravir)的EUA申请材料,FDA组织11月30日讨论,历时1个月19天(7周+2天);
辉瑞于11月16日提交新冠药物Paxlovid的EUA申请材料,按照时间线推算,若FDA审批速度加快,12月圣诞节前后能组织讨论EUA授权问题;
2、PAXLOVID:辉瑞研发的新冠口服药剂Paxlovid主要通过抑制新冠病毒的3CL蛋白酶活性来影响病毒在人体中的复制增殖,达到治疗新冠的效果。辉瑞公司11月公布的该药物Ⅱ/Ⅲ期临床试验中期分析结果显示,口服该药能降低89%的住院和死亡风险。
3、有望覆盖全球约53%的人口
1)辉瑞公司首席科学官MikaelDolsten说,辉瑞计划在11月寻求美国食品药品监督管理局(FDA)批准该药物,如果获批,辉瑞可能在今年交付。如果获批,按照辉瑞CEO的预测,Paxlovid明年有望实现8000万疗程的生产,美国政府已经火急火燎地采购了1000万疗程的Paxlovid如果按照美国政府1000万疗程52.9亿美金的采购价格估算,意味着明年辉瑞光Paxlovid的销售额就有可能突破423亿美,市场空间巨大。
2)值得一提的是,辉瑞新冠口服药允许仿制药生产。此次辉瑞将直接针对发达国家自行生产和销售Paxlovid,而针对部分中高收入国家、大部分中低收入国家和低收入国家将通过授权许可的合格仿制药企业来生产销售Paxlovid的仿制药。
辉瑞公司表示,已就该新冠药物与联合国支持的公共卫生组织“药品专利池”(MPP)达成自愿许可协议,获得MPP授权的合格仿制药生产商将能向95个国家提供该药,覆盖全球约53%的人口。
这样一来,不仅有望加速人类战胜新冠的进程,还给整个疫情产业链带来了全新的机会。
4、原料药的主要中间体
该药由小分子药物PF-07321332和低剂量的利托那韦组成,前者是针对新冠病毒主蛋白酶的抑制剂,利托那韦则是抗病毒药增效剂,此前曾用于抗艾滋病病毒。其中PF-7321332需要使用柠檬醛下游2-异戊烯醇做到龙卡酸酐。
另外,在中金公司12月发布的一篇报告中重点提到了合成PF的中间体卡龙酸酐,并且不管是菊酸路线还是异戊烯醇路线,都绕不开卡龙酸酐;
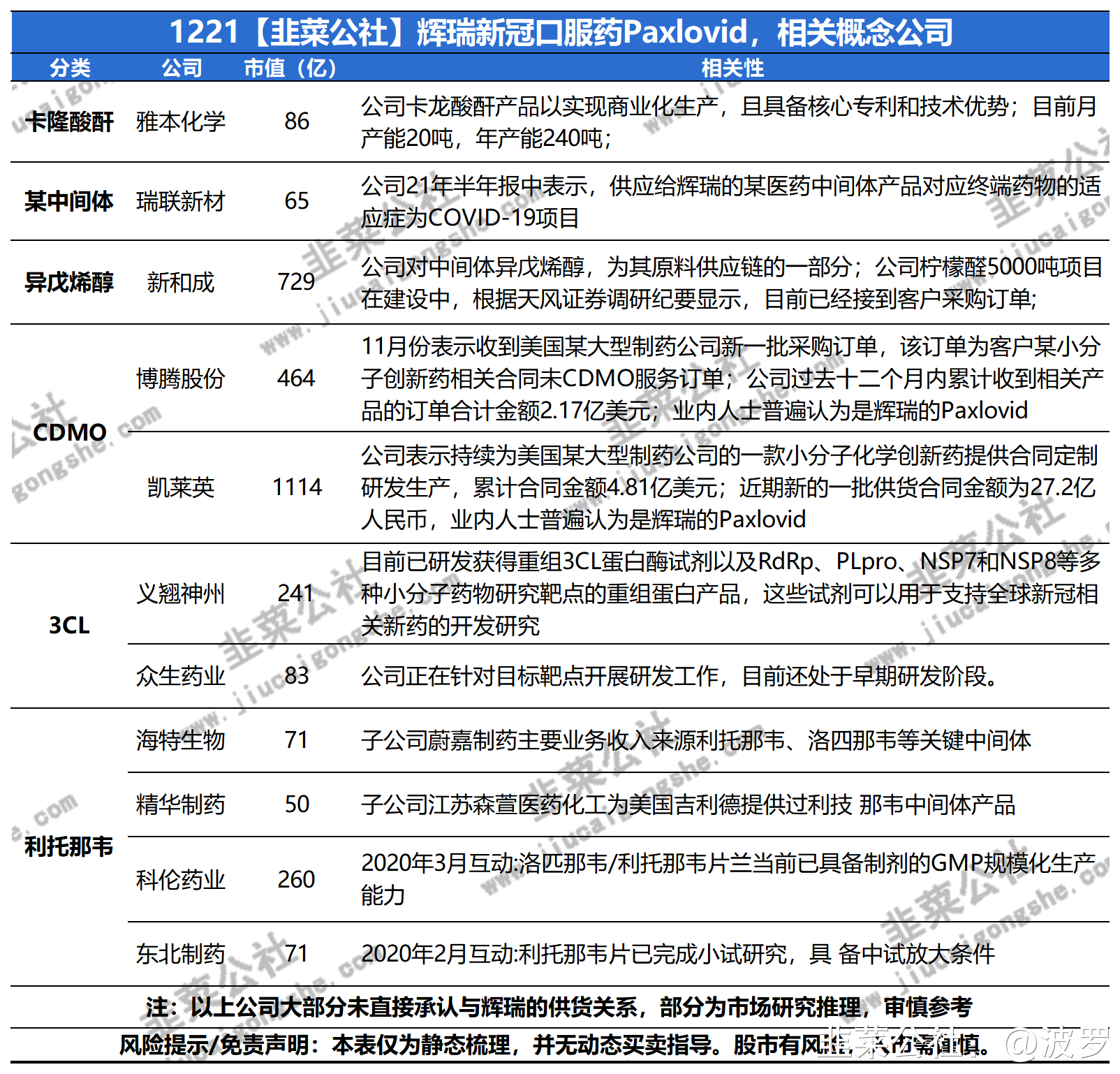
相关公司



- 1
- 2













