据了解,Tempest是一家临床阶段肿瘤公司,致力于将肿瘤靶向和免疫介导机制结合起来开发小分子,这类小分子可能具有治疗多种肿瘤的潜力。
Tempest Therapeutics于前日发布新闻稿,表示将于昨日盘前报告TPST-1120 一线肝细胞癌全球随机组合研究的新数据和更新数据,并进行电话会议直播。
日内,Tempest公布了其研发的“TPST-1120”在临床试验中获得的最新积极数据结果。据了解,TPST-1120是一种口服、选择性PPARα小分子拮抗剂。
在1b/2期临床研究中,TPST-1120与atezolizumab和bevacizumab组成了“三联治疗方案”,与只有atezolizumab和bevacizumab“标准治疗方案”对照组进行了随机比较。
Tempest在最新的声明中称,“三联”在多个类别方面均有改善,印证了其4月份积极的初步结果。具体数据显示,三联组经确认的客观缓解率(ORR)为30%,对照组为13.3%。
公司CEO Stephen Brady称,“对更成熟的临床数据进行的全面分析表明,与单独的标准治疗方案相比,三联疗法的早期和中期分析具有更大的益处,预计原因是TPST-1120在其中的作用机制。”
三联疗法:TPST-1120与标准疗法(抗PD-L1抗体atezolizumab和抗VEGF抗体Avastin)联用
TPST-1120与标准治疗方案联用,在无法切除或转移性HCC患者的一线治疗中,显著改善客观缓解率并有良好的安全性。
TPST-1120是一种口服、选择性PPARa小分子拮抗剂,它可直接杀死肿瘤细胞,并靶向肿瘤微环境中的抑制性免疫通路。这两种类型中的靶向细胞皆依赖脂肪酸代谢,该代谢过程由PPARa转录因子调节
国内方面:
神州细胞688520值得关注
根据调研神州细胞:
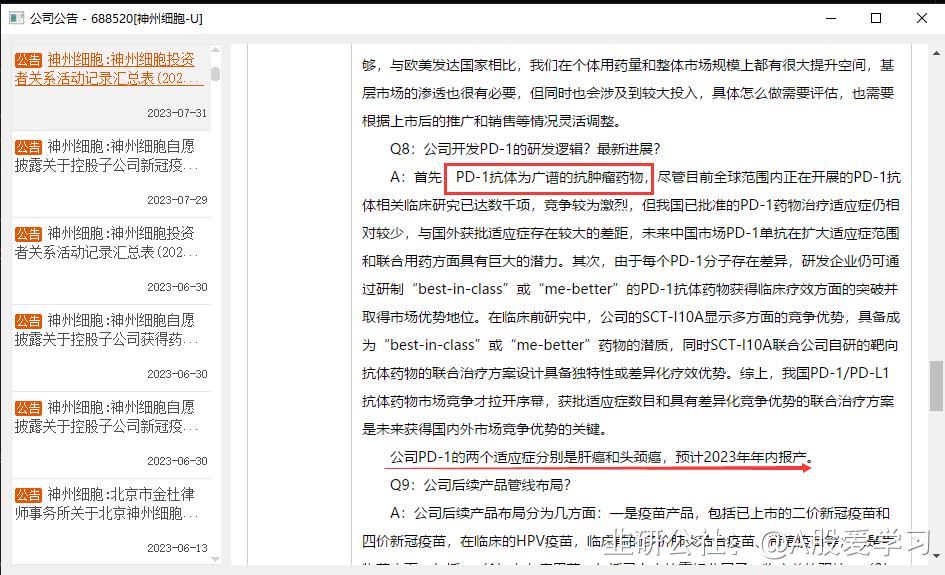
PD-1抗体为广谱的抗肿瘤药物,尽管目前全球范围内正在开展的PD-1抗体相关临床研完已达数千项,竞争较为激烈,但我国已批准的PD-1药物治疗适应症仍相对较少,与国外获批适应症存在较大的差距,未来中国市场PD-1单抗在扩大适应症范围和联台用药方面具有巨大的潜力。
其次,由于每个PD-1分子存在差异,研发企业仍可通过研制“best-in-class”或“me-better”的PD-1抗体药物获得临床疗效方面的突破并取得市场优势地位。
在临床前研完中,公司的SCT-I10A显示多方面的竞争优势,具备成为“best-in-class”或“me-better”药物的潜质,同时SCT-I10A联合公司自研的靶向抗体药物的联合治疗方案设计具备独特性或差异化疗效优势。
综上,我国PD-1/PD-L1抗体药物市场竞争才拉开序幕,获批适应症数目和具有差异化竞争优势的联合治疗方案是未来获得国内外市场竞争优势的关键。
公司PD-1的两个适应症分别是肝癌和头颈癌,预计2023年年内报产!



- 1
- 2













