近期官媒暖风频吹,强调新冠不可怕是自限性疾病,被市场视为是开放前的心理按摩准备,而如果一旦开放,按目前传播力度,全国至少一半的以上的国民感染,感染后绝大部分都是轻症,发烧在家,按国外经验,主要检测手段会从测核酸变为居家自测抗原,按国外经验,一个感染流程基本要测3-4次,抗原检测试剂需求将引来巨大增量!、
一、三种新冠检测手段:(目前以核酸检测为主,策是放开抗原检测)
1、核酸检测:窗口期靠前,同时特异性较高,可以用于早期发现病毒感染,是目前国内主要的检测手段,也是目前新冠患者的确诊标准之一,但是核酸检测的缺点是开展条件较高,检测需要的时间较长。
2、免疫学检测:窗口期靠后,但是检测易于开展且检测时间比较短,可以用于大规模的阳性人群筛查、治疗康复评估等。
3、抗原检测:在全球多国已有广泛使用,相较于核酸检测方法,其出结果速度更快,且价格低廉。
二、《新冠病毒抗原检测应用方案(试行)》
国W院应对冠状病毒肺炎疫情联防联控机制综合组决定在核酸检测基础上,增加抗原检测作为补充,社区居民有自我检测需求的,可通过零售药店、网络销售平台等渠道,自行购买抗原检测试剂进行自测。
《方案》规定了抗原检测的适用人群:一是到基层医疗卫生机构就诊,伴有呼吸道、发热等症状且出现症状5天以内的人员;二是隔离观察人员,包括居家隔离观察、密接和次密接、入境隔离观察、封控区和管控区内的人员;三是有抗原自我检测需求的社区居民。同时,明确了3类人群进行抗原检测需满足的主要条件、检测试剂的获得渠道,制定了检测发现阳性后的处置管理流程,促进抗原检测与核酸检测相衔接。
居家隔离观察、密接和次密接、入境隔离观察、封控区和管控区内的人员,由相关管理部门(如社区、村镇、隔离点等)做好组织管理。在隔离观察期按照现行的有关防控方案要求开展核酸检测,并在前5天每天进行一次抗原自测。
三、新冠抗原家用自测测试剂盒市场空间测算
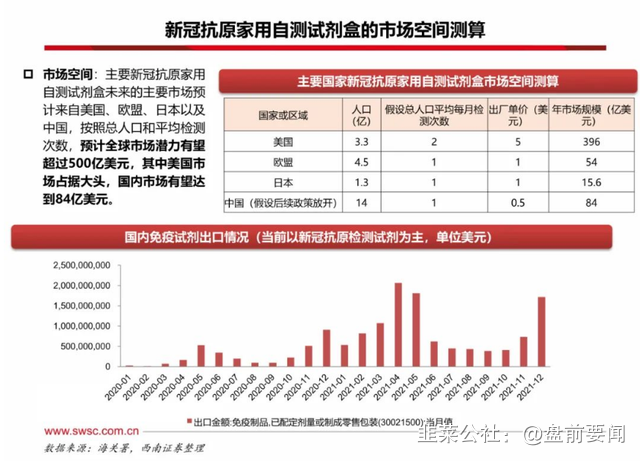
这是之前的测算,一旦开放,远不止一个月一次的抗原检测,新冠变异株极多,国外许多人感染了多次新冠,可见市场空间很大
四、哪些上市公司获批
九安医疗:目前累计收到新冠抗原家用自测试剂盒产品货款4.65亿美元
东方生物:抗原自测试剂获得美国FDA EUA授权指定供应
万孚生物:2022年1月11日公告,公司抗原自测产品完成欧盟CE认证的公告
明德生物:2021年12月6日互动平台,新冠抗原自测产品已获得欧盟CE认证
热景生物:2022年1月14日公告,抗原自测产品已于2021年8月获得欧盟CE认证
安旭生物:2022年1月14日公告,抗原鼻腔检测试剂(自测)于近日取得欧盟CE认证
奥泰生物:2021年11月23日互动平台,抗原检测试剂可在欧盟市场进行全面销售
塞力医疗:2022年1月17日互动平台,抗原试剂盒取得欧盟CE认证
东方生物:2021年8月3日公告,抗原自测试剂获得欧盟CE认证
硕世生物:
华大基因:2022年2月7日公告,子公司新冠抗原自测产品获欧盟CE证书
亚辉龙:2021年12月19日公告,抗原自测检测试剂盒获得欧盟CE认证
迈克生物:2020年12月4日公告,抗原检测试剂盒(胶体金法)获欧盟CE认证
博拓生物:2021年11月22日互动平台,抗原家庭自测检测试剂已取得CE证书
迪安诊断:2021年12月27日公告,抗原检测试剂盒被列入欧盟通用白名单
达安基因:2021年4月21日互动平台,中山生物开发的抗原检测试剂盒(胶体金法),已于2020年09月14日获得CE认证
乐普医疗:2021年6月22日公告,抗原自测试剂盒获得欧盟CE认证
新产业:2022年3月9日互动平台,抗原检测试剂盒(胶体金法)已于2021年9月取得CE准入资格
基蛋生物:2021年8月2日公告,抗原自测检测试剂盒获得欧盟CE认证
之江生物:2022年1月18日公告,抗原检测试剂盒近期获得四项欧盟CE认证
美康生物:2021年3月24日官微,抗原检测试剂盒在取得欧盟CE证书之后,入选商务部《取得国外标准认证或注册的医疗物资生产企业清单》
九强生物:2020年12月24日公告,抗原检测试剂盒产品取得欧盟CE准入资格
(来自韭研公社APP)



- 1
- 2













